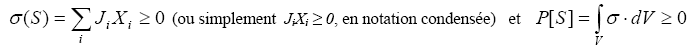a. La thermodynamique non linéaire
L’école de Bruxelles s’est construite autour du physicien Théophile De Donder (1872-1957), auteur d’un ouvrage important sur l’affinité chimique en 1927
1541
. La réflexion sur les phénomènes irréversibles est au cœur de l’activité du groupe, en particulier d’Ilya Prigogine (1917-2003), destiné à devenir le leader de cette école. Cet intérêt est très clairement exprimé dans son ouvrage de 1947 :
‘"Une thermodynamique de la réaction chimique sera nécessairement une thermodynamique des phénomènes irréversibles […]’
‘Quand on réfléchit à ces différents points, on est amené inévitablement à la conclusion que la thermodynamique classique constitue une doctrine admirable sans aucun doute, mais
fragmentaire, et que ce caractère fragmentaire provient de ce qu’elle n’est applicable qu’aux seuls états d’équilibre des systèmes fermés.
Il faut dès lors chercher à fonder une théorie plus vaste qui englobe les états de non-équilibre et les états d’équilibre."
1542
’
On peut constater deux choses. Les états oscillants (qui sont des états de non-équilibre) trouvent leur place dans le projet. Dans une moindre mesure, il s’agit également d’un programme pour la thermodynamique parallèle aux ambitions d’Andronov qui souhaitait construire une théorie pour les oscillations englobant l’essentiel des oscillations.
Ici, l’objectif affiché n’est pas de trouver un arrangement à la thermodynamique classique, mais de fonder une nouvelle thermodynamique, valable pour des systèmes ouverts et prenant en compte l’irréversibilité. De la même manière que la thermodynamique macroscopique classique est phénoménologique, tous ces développements sont de l’ordre de la phénoménologie.
La première étape dans cette démarche a été de construire une thermodynamique linéaire des processus irréversibles (ou encore, thermodynamique proche de l’équilibre). L’école de Bruxelles, en même temps que le physicien norvégien Lars Onsager (1903-1976), a défini l’essentiel des notions de cette thermodynamique. Onsager a établi les relations dites de réciprocité en 1931
1543
. Prigogine a démontré le théorème de la production minimale d’entropie. Le tout repose sur l’hypothèse de l’équilibre local : l’état thermodynamique local est voisin d’un état d’équilibre.
Le système dans sa globalité évolue de manière irréversible et localement on applique les équations valables pour l’état d’équilibre. Dans ce cas il est possible de définir avec Onsager, des grandeurs flux et forces généralisées
1544
. L’autre concept central est la notion de production d’entropie. Le théorème de Prigogine stipule qu’un système physicochimique soumis à de faibles contraintes permanentes (pour rester dans le cadre d’une approximation du premier ordre), interdisant l’accès à l’équilibre mais seulement un état stationnaire de non-équilibre, s’accompagne d’une production d’entropie décroissante qui atteint sa valeur minimale à l’état stationnaire.
Les hypothèses retenues correspondent à une relation linéaire entre les grandeurs flux et force, grandeurs qui caractérisent la thermodynamique proche de l’équilibre
1545
.
L’extension dans le domaine éloigné de l’équilibre engage à reconsidérer ce point de vue. Le cadre du développement de ces travaux est évidement celui des systèmes ouverts. Paul limite et George Van Lerberghe avaient dès les années 1930 proposé une théorie des systèmes ouverts, mais insatisfaisante aux yeux de Prigogine
1546
. Dans son ouvrage de 1947 Prigogine annonce que le point de départ, l’hypothèse d’équilibre local, reste le même
1547
. Le travail de longue haleine se poursuit les années suivantes grâce à une collaboration entre Prigogine et limite notamment. La difficulté est bien supérieure au cas linéaire car il est impossible de construire un principe variationnel général, autrement dit rien ne remplace simplement la production d’entropie et le théorème de Prigogine.
L’aboutissement
1548
est la publication de leur traité commun : Structure, stabilité et fluctuations en 1971. L’objectif est de chercher à dépasser les approximations du linéaire c’est-à-dire de produire une "extension de la thermodynamique au domaine non linéaire"
1549
. Leur ambition est d’englober ces situations non linéaires et les questions d’instabilités connues, apparaissant en hydrodynamique notamment.
Le titre de l’ouvrage donne trois des éléments clés abordés par limite et Prigogine pour les fondements d’une telle physique macroscopique. Car il s’agit bien là du développement de tout un pan de la physique macroscopique quelque peu délaissé par la communauté physicienne. Une seule phrase suffit à montrer l’intrication des trois éléments :
‘"[…] une nouvelle ‘structure’ est toujours la conséquence d’une instabilité. Elle est engendrée par une fluctuation."
1550
’
Les auteurs distinguent deux types de structures : les structures d’équilibres, bien connues dans le cadre de la thermodynamique classique (l’exemple le plus simple étant le cristal) et les structures dissipatives. Cette dernière notion deviendra le symbole du travail de limite et surtout de Prigogine.
Autour de 1970, en une sorte de préliminaire à l’interaction entre ces théories et la réaction de Belousov-Zhabotinsky se produit une convergence conceptuelle entre les théories de la stabilité thermodynamique, les mathématiques de Lyapounov et les cycles limites de Poincaré, associée à un croisement avec les expériences chimiques et numériques.